Dale una cerveza a un hombre y será feliz un rato.
Enséñale a hacer cerveza y será feliz toda la vida
Aristarco de Birmingham (Cervezomicón 8:12)
Video-curso

Videos cursos de cómo hacer cerveza
Aprende a hacer cerveza con un curso profesional en video. [¡plink!]
DOBLE-IPA

Técnicas de elaboración de una doble IPA
Cómo clonar la Pliny de Elder de Russian River [¡plink!]
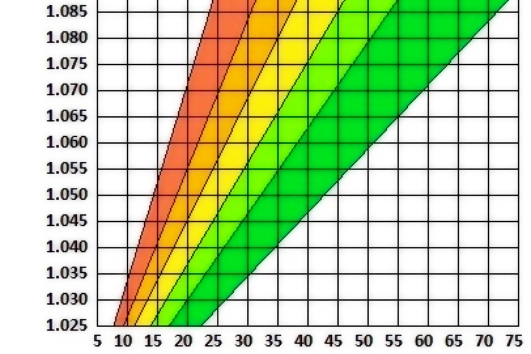
LEVADURA

Starters, starters, starters
Guía para entender cómo y cuánta levadura poner en tu mosto [¡plink!]
SCOTTISH ALES

Scottish Ales | El estilo fantasma
Repaso a la «historia» de las cervezas escocesas [¡plink!]
agua (II)

Introducción a la química (by The Kruger Brewer)
Agua para cerveza, todo lo que quieres saber [¡plink!]
mitos jombrigüer

Los seis mitos más extendidos entre los jombrigüeres
Denny Conn nos habla sobre creencias infundadas [¡plink!]
macerado

Las cuatro palancas del macerado
Entendamos lo que ocurre cuando ponemos la malta molida en el agua caliente [¡plink!]
MATEMÁTICAS

Cálculo de IBUs
Para que tus cervezas tengan el amargor adecuado, necesitas manejar los IBU [¡plink!]
decocción

En defensa de la decocción
La perspectiva de un purista sobre un método ancestral [¡plink!]
porter Vs. stout

Esquizofrenia paranoide
¿Son las cervezas porter y las stouts dos cosas diferentes? [¡plink!]
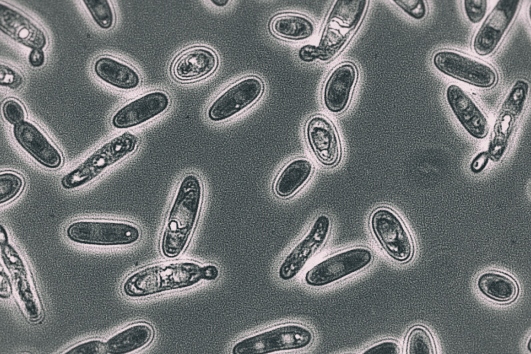
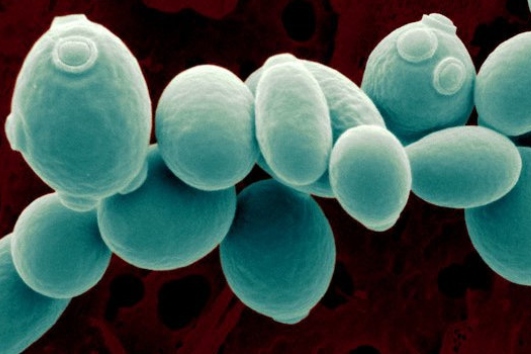
levaduras

La dura vida de las levaduras
Conozcamos, más de cerca, a nuestra pequeñas amiguitas [¡plink!]
weizenbier

Historia y elaboración de la cerveza de trigo bávara
Recorrido histórico y por la teoría de elaboración de la weizenbier [¡plink!]
fermentación

Luchando contra el CALOR
Qué hacer si no tienes control de temperatura en las fermentaciones [¡plink!]
maltas

¿Es malta Crystal o Caramelo?
Se suelen confundir las maltas «Crystal» y «Caramel» y vamos a dar luz al asunto [¡plink!]
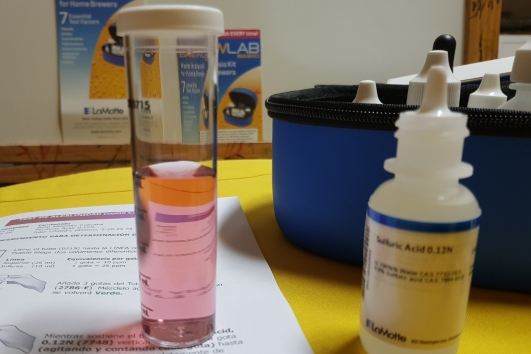
DEFECTOS

¡Con el azufre hemos topado, amigo jombrigüer!
Cómo evitar los sabores no deseados derivados de los compuestos azufrados [¡plink!]
vienna lager

Cómo elaborar la cerveza Marzën / Oktoberfest
Origen y elaboración de este estilo histórico [¡plink!]
carbonatación

Teoría de la refermentación en botella
Claves para conseguir el «¡pssst!» que suena al abrir una botella de cerveza [¡plink!]
adjuntos

¿El arroz es ‘güeno’? | Macerado asistido
Como usar algo más que malta en un macerado para mejorar la cerveza [¡plink!]
maltas

¿El secreto está en la malta?
Conceptos básicos sobre cómo se hace la malta, características y tipos [¡plink!]
PASTRY BEERS

Cervezas Pasteleras o «Pastry Beers»
Cómo ponerle cosas raras y dulces a tu cerveza sin morir en el intento [¡plink!]
macerado

Parti-Gyle, divide y bebe más (variedad)
Técnica para elaborar diferentes cervezas de un único macerado [¡plink!]
macerado

Historia y evolución de los sistemas de macerado
Sistemas de maceración históricos. Y también qué es RIMS, HERMS y DIMS [¡plink!]
adjuntos

Cereales sin maltear en el macerado
The Kruger Brewer nos cuenta el procedimiento estándar para macerar cualquier cereal no malteado [¡plink!]
ZIROPITEKO

Cómo hacer un tirador de cerveza con una nevera de picnic
Un poco de bricolaje cervecero para beber tu cerveza lejos de casa [¡plink!]
blending

Mezcla de cervezas
Vemos las posibilidades de mezclar cervezas para mejorar el resultado [¡plink!]
opinión

¿Qué es la cerveza artesanal o artesana?
El viejo debate que vuelve en bucle continuamente [¡plink!]
estilos
Introducción a los estilos cerveceros
Qué son los estilos cerveceros y porqué es útil conocerlos [¡plink!]